Truyền thông về An toàn Thuốc của FDA: FDA khuyến cáo không nên sử dụng Revatio (sildenafil) ở trẻ em bị tăng huyết áp động mạch phổi
Thông báo An toàn
[8-30-2012] Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) khuyến cáo không nên kê đơn Revatio (sildenafil) cho trẻ em (từ 1 đến 17 tuổi) để điều trị tăng huyết áp động mạch phổi (PAH; áp lực cao trong mạch máu dẫn đến phổi). Khuyến cáo không sử dụng này dựa trên một thử nghiệm lâm sàng dài hạn gần đây cho thấy: (1) trẻ em dùng Revatio liều cao có nguy cơ tử vong cao hơn so với trẻ em dùng liều thấp và (2) trẻ em dùng Revatio liều thấp là không có hiệu quả trong việc cải thiện khả năng tập thể dục. 1 Hầu hết các trường hợp tử vong là do tăng áp động mạch phổi và suy tim, đây là những nguyên nhân phổ biến nhất gây tử vong ở trẻ em bị PAH.
Sự thật về sildenafil
- Một chất ức chế phosphodiesterase-5 được sử dụng để điều trị tăng huyết áp động mạch phổi bằng cách làm giãn mạch máu trong phổi để giảm huyết áp.
- Cũng được bán trên thị trường trong sản phẩm theo toa Viagra, một loại thuốc dành cho nam giới trưởng thành bị rối loạn chức năng cương dương (không thể đạt được hoặc duy trì sự cương cứng). Tại thời điểm này, FDA không tin rằng mối quan tâm an toàn này áp dụng cho việc sử dụng Viagra, do sự khác biệt về dân số bệnh nhân và các chế độ dùng thuốc được khuyến nghị khác nhau.
Revatio chưa bao giờ được chấp thuận để điều trị PAH ở trẻ em và theo thông tin thử nghiệm lâm sàng mới, việc sử dụng thuốc ngoài nhãn (không được FDA chấp thuận) không được khuyến khích ở bệnh nhân nhi. Thông tin mới sau đây đang được thêm vào nhãn thuốc Revatio:
- Một cảnh báo mới cho biết việc sử dụng Revatio không được khuyến khích ở bệnh nhân nhi
- Kết quả của thử nghiệm Revatio ở bệnh nhi
Revatio được phê duyệt để cải thiện khả năng tập thể dục và trì hoãn sự xấu đi trên lâm sàng của PAH ở bệnh nhân người lớn ( WHO Nhóm I). Nhãn Revatio hiện tại khuyến cáo tránh dùng liều cao hơn 20 mg, ba lần một ngày. Ảnh hưởng của Revatio đối với nguy cơ tử vong khi sử dụng lâu dài ở người lớn chưa được biết rõ; FDA đang yêu cầu nhà sản xuất Revatio (Pfizer) đánh giá tác dụng của Revatio đối với nguy cơ tử vong ở người lớn với PAH.
Thông tin bổ sung cho bệnh nhân
- Không thay đổi liều Revatio của bạn hoặc ngừng dùng Revatio mà không nói chuyện với chuyên gia chăm sóc sức khỏe của bạn.
- Thảo luận bất kỳ câu hỏi nào bạn có về Revatio với chuyên gia chăm sóc sức khỏe của bạn.
- Báo cáo bất kỳ tác dụng phụ nào bạn gặp phải cho chương trình FDA MedWatch bằng cách sử dụng thông tin trong ô “Liên hệ với FDA” ở cuối trang.
Thông tin bổ sung cho các chuyên gia chăm sóc sức khỏe
- Sử dụng Revatio, đặc biệt là sử dụng mãn tính, không được khuyến khích ở trẻ em. Nguy cơ tử vong cao hơn bất ngờ được tìm thấy ở bệnh nhi dùng Revatio liều cao khi so sánh với bệnh nhi dùng liều thấp. [xem Tóm tắt Dữ liệu ]
- Liều khuyến cáo tối đa của Revatio cho bệnh nhân người lớn bị PAH là 20 mg ba lần một ngày.
- Báo cáo các sự kiện bất lợi liên quan đến Revatio cho chương trình FDA MedWatch, sử dụng thông tin trong hộp “Liên hệ với FDA” ở cuối trang.
Trong một thử nghiệm lâm sàng ngẫu nhiên, mù đôi, đa trung tâm, đối chứng với giả dược, nhóm song song, liều lượng, 234 bệnh nhân mắc PAH, từ 1 đến 17 tuổi, được chọn ngẫu nhiên thành thấp, trung bình hoặc cao- liều Revatio (sildenafil; dùng ba lần mỗi ngày) hoặc giả dược trong 16 tuần điều trị. Hầu hết bệnh nhân có các triệu chứng nhẹ đến trung bình lúc ban đầu. Liều thực tế được sử dụng phụ thuộc vào trọng lượng cơ thể.
Mục tiêu chính của thử nghiệm là đánh giá tác động của Revatio đối với khả năng gắng sức như được đo bằng Bài kiểm tra bài tập về tim phổi (CPET) ở những bệnh nhân phát triển có thể thực hiện bài kiểm tra (n = 115). Việc sử dụng Revatio không dẫn đến sự cải thiện có ý nghĩa thống kê về khả năng tập thể dục ở những bệnh nhân này.
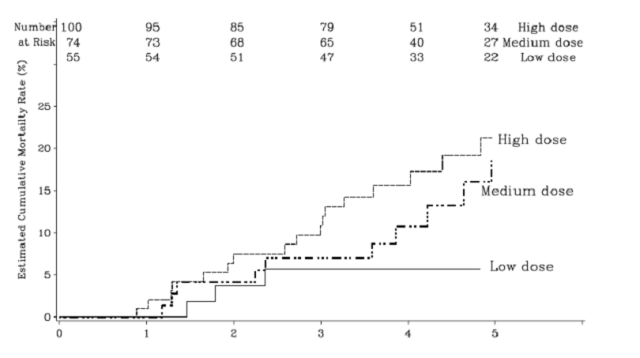
Sau khi hoàn thành thử nghiệm lâm sàng có đối chứng kéo dài 16 tuần, các bệnh nhân ngẫu nhiên sử dụng Revatio vẫn sử dụng cùng liều Revatio; những bệnh nhân ban đầu được chọn ngẫu nhiên với giả dược được phân ngẫu nhiên lại thành Revatio liều thấp, trung bình hoặc cao. Sau khi tất cả các bệnh nhân hoàn thành 16 tuần theo dõi trong thử nghiệm lâm sàng có kiểm soát, người mù đã được phá vỡ và điều chỉnh liều theo chỉ định lâm sàng. Bệnh nhân được theo dõi trong thời gian trung bình là 3 năm (từ 0 đến 7 năm). Tỷ lệ tử vong trong quá trình thử nghiệm lâm sàng dài hạn, như một hàm của liều lượng được chỉ định ban đầu, được thể hiện trong hình bên dưới.
Hình: biểu đồ tỷ lệ tử vong trong thử nghiệm lâm sàng ở trẻ em dưới dạng hàm của liều Revatio.
Một tác động trực tiếp liên quan đến liều lượng trên tỷ lệ tử vong đã được quan sát thấy với liều cao nhất có kết quả tồi tệ nhất. Tỷ lệ nguy cơ đối với liều cao so với liều thấp là 3,5 (p = 0,015). Các trường hợp tử vong lần đầu tiên được quan sát thấy sau khoảng 1 năm, sau đó xảy ra với tỷ lệ khá ổn định trong mỗi nhóm. Nguyên nhân tử vong là điển hình của bệnh nhân tăng áp động mạch phổi.
Do những rủi ro này, việc sử dụng Revatio không được khuyến cáo ở trẻ em. Một cảnh báo mới chống lại việc sử dụng Revatio ở bệnh nhi đang được thêm vào nhãn thuốc Revatio.
Người giới thiệu
- Barst RJ, Ivy DD, Gaitan G, et al. Một nghiên cứu ngẫu nhiên, mù đôi, có đối chứng với giả dược, theo liều lượng của sildenafil citrate đường uống ở trẻ em chưa từng điều trị bị tăng huyết áp động mạch phổi. Lưu hành 2012; 125: 324-334.
Comments
Post a Comment